-
Perhatikan reaksi pembentukan amonia berikut:
N2(g) + H2(g) ⇌ NH3(g)
Pada suhu dan tekanan yang sama, perbandingan volume gas-gas yang terlibat dalam reaksi tersebut secara berurutan adalah....
-
Suatu cuplikan yang mengandung pirit (FeS) seberat 88 gram bereaksi dengan HCl sehingga menghasilkan FeCl2 dan gas H2S. Jika dihasilkan produk berupa 15 L H2S yang diukur pada saat 2,5 L gas Nitrogen bermassa 3,5 gram, maka persentase massa FeS pada cuplikan tersebut adalah....
(Ar Fe = 56, Cl = 35,5, H = 1, S = 32, N = 14)
-
Pernyataan yang benar tentang H3PO4, H2SO4, dan HClO4 adalah ….
HClO4 merupakan oksidator kuat.
H3PO4 merupakan asam terlemah.
Pada konsentrasi 0,1 M larutan H2SO4 memiliki pH terendah.
Na3PO4 merupakan basa paling kuat dibandingkan Na2SO4 dan NaClO4.
-
-
Larutan A memiliki konsentrasi Na2SO4 sebesar 0,2 M, sedangkan larutan B memiliki konsentrasi sukrosa sebesar 0,5 M. Perbandingan tekanan osmotik larutan A terhadap larutan B pada temperatur yang sama adalah ....
-
Sebanyak 4,16 gram gas A terbentuk dari reaksi antara 1 liter gas NO2 dan gas O2 berlebih menurut reaksi
4NO2(g) + O2(g) → 2A(g)
Jika reaksi tersebut berlangsung pada suhu 300C dengan tekanan 2 atm, maka massa molekul relatif gas A adalah .... (R=0,082 liter atm/mol K)
-
Diketahui reaksi redoks (belum setara):
PbSO4(s)+H2O(l)→Pb(s)+PbO2(s)+H2SO4(aq)
Pernyataan berikut ini yang benar adalah ....
- PbSO4 berperan sebagai oksidator
- PbSO4 berperan sebagai reduktor
- Pada akhir reaksi pH laturan lebih kecil dari 7
- Perbandingan mol PbSO4 terhadap H2O adalah 1:2
-
Proses pemurnian belerang yang dilakukan oleh Frasch dikenal juga dengan proses penambangan sumur panas. Konsep kerjanya adalah dengan mengalirkan air panas kedalam sumur galian yang terdapat deposit belerang, sehingga belerang akan meleleh dan mengapung pada permukaan air. Namun diawal proses ini, Frasch mengalami permasalahan. Suhu tertinggi dari air panas adalah 100oC, namun belerang memiliki titik lebur pada suhu 101,6o C.
Analisis, cara manakah di bawah ini yang paling tepat untuk menyelesaikan masalah yang dihadapai Frasch? (diketahui
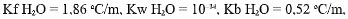 Ar S = 32 g/mol, Ar H = 1 g/mol, O = 16 g/mol).
Ar S = 32 g/mol, Ar H = 1 g/mol, O = 16 g/mol). -
SEBAB
-
Skor
/10